ดร.สุทธิพงษ์ ชูจันทร์, รศ.ดร.ภญ.จุฑามาศ สัตยวิวัฒน์
ห้องปฏิบัติการวิจัยเภสัชวิทยา สถาบันวิจัยจุฬาภรณ์
และศูนย์ความเป็นเลิศด้านอนามัยสิ่งแวดล้อมและพิษวิทยา
ไวรัสนิปาห์ (Nipah virus) เป็นไวรัสในสกุล Henipavirus วงศ์ Paramyxoviridae ติดต่อจากสัตว์สู่คน ซึ่งมีค้างคาวผลไม้เป็นแหล่งรังโรคหลัก หรืออาจจะพบได้ในสุกร สุนัข แมว ม้า หรือแพะ โดยการสัมผัสใกล้ชิดกับค้างคาวหรือสัตว์ติดเชื้อ ผ่านทางสารคัดหลั่ง น้ำลาย มูล และเสมหะของสัตว์ที่ติดเชื้อ การติดเชื้อไวรัสนิปาห์ในคนจะมีลักษณะคล้ายไข้หวัดใหญ่ คือ มีไข้สูง เจ็บคอ ไอ ปวดเมื่อยตามตัว และอ่อนเพลีย หลังจากรับเชื้อ 4-14 วัน หรืออาจจะก่อให้เกิดอาการรุนแรงทั้งทางระบบทางเดินหายใจและระบบประสาทส่วนกลาง เช่น ปอดอักเสบหรือสมองอักเสบเฉียบพลัน ซึ่งนำไปสู่อัตราการเสียชีวิตที่สูงถึงร้อยละ 40-75
โรคติดเชื้อไวรัสนิปาห์ จัดเป็นโรคอุบัติใหม่จากสัตว์สู่คนที่สร้างความกังวลต่อระบบสาธารณสุขทั่วโลกรวมถึงประเทศไทย เนื่องจากการติดเชื้อมีอัตราการเสียชีวิตสูง ในประเทศไทยพบว่า มีเชื้อไวรัสนิปาห์ในค้างคาว แต่ไม่พบว่า มีการระบาดสู่สัตว์เลี้ยงลูกด้วยน้ำนมและมนุษย์ ดังนั้น การควบคุมโรคจึงมุ่งเน้นไปที่การป้องกัน การเฝ้าระวัง และการจัดการผู้ป่วยตามหลักการแพทย์แผนปัจจุบันเป็นหลัก ปัจจุบันยังไม่มีวัคซีนป้องกันและยาที่ใช้รักษาได้อย่างจำเพาะ จึงยังคงเป็นการรักษาแบบประคับประคองอาการ
ในปัจจุบัน ภายใต้สถานการณ์ดังกล่าว ความสนใจต่อสมุนไพรและสารจากธรรมชาติในฐานะแหล่งของสารออกฤทธิ์ทางชีวภาพจึงเพิ่มมากขึ้น โดยจากการติดตามบทความวิจัยพบว่า มีสมุนไพรหลายชนิดที่มีฤทธิ์เสริมสร้างภูมิคุ้มกันและบรรเทาอาการจากการติดเชื้อไวรัสนิปาห์ เช่น กระชายขาว ขมิ้นชัน ฟ้าทะลายโจร และพืชสมุนไพรชนิดอื่นๆ เป็นต้น
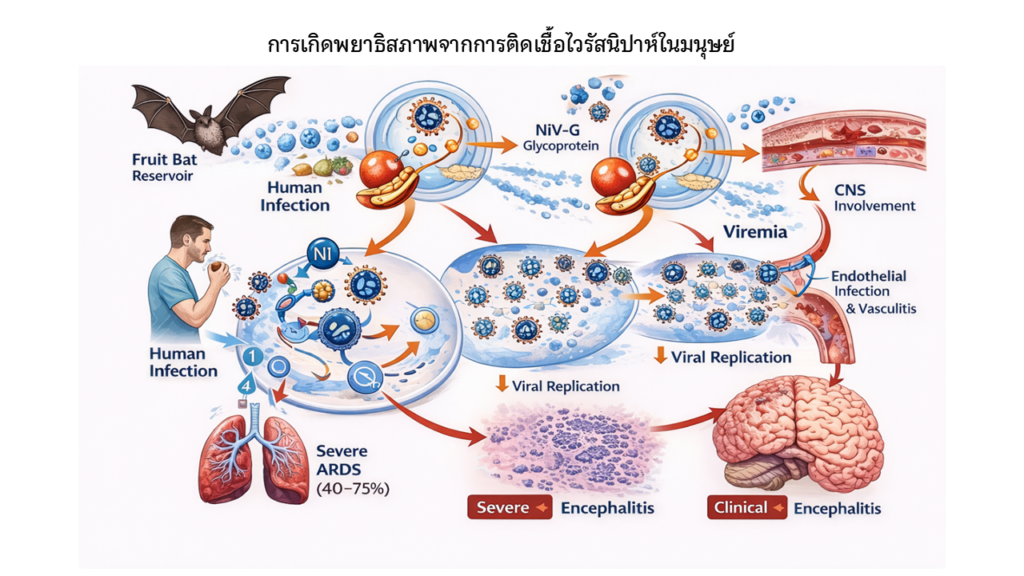
ภาพที่ 1 กลไกการเกิดโรคจากการติดเชื้อไวรัสนิปาห์ในมนุษย์ (Pathogenesis of Nipah Virus Infection in Humans)
ภาพนี้ แสดงลำดับขั้นของการติดเชื้อและการดำเนินโรคของไวรัสนิปาห์ (Nipah virus; NiV) ในมนุษย์ โดยไวรัสนิปาห์ มีค้างคาวกินผลไม้ (สกุล Pteropus) เป็นแหล่งรังโรคตามธรรมชาติ การติดต่อสู่มนุษย์สามารถเกิดขึ้นได้จากการสัมผัสโดยตรงกับค้างคาวหรือสารคัดหลั่ง การบริโภคอาหารหรือผลไม้ที่ปนเปื้อน โดยหลังจากไวรัสเข้าสู่ร่างกาย ไวรัสนิปาห์จะจับกับเซลล์เจ้าบ้านผ่านโปรตีน G (NiV-G glycoprotein) ซึ่งจับกับตัวรับ ephrin-B2 และ ephrin-B3 ที่พบได้บนเซลล์เยื่อบุทางเดินหายใจ เซลล์บุผนังหลอดเลือด และเซลล์ประสาท จากนั้น โปรตีน F ของไวรัสจะทำหน้าที่ช่วยให้เกิดการหลอมรวมของเยื่อหุ้ม ทำให้ไวรัสสามารถเข้าสู่เซลล์และเริ่มกระบวนการเพิ่มจำนวนของไวรัส (viral replication) ภายในเซลล์บริเวณไซโทพลาสซึม ไวรัสที่เพิ่มจำนวนแล้ว จะแพร่กระจายเข้าสู่กระแสเลือด (viremia) ส่งผลให้เกิดการติดเชื้อในเซลล์บุผนังหลอดเลือดทั่วร่างกาย ก่อให้เกิดภาวะหลอดเลือดอักเสบ (vasculitis) ความเสียหายของผนังหลอดเลือด และการเพิ่มความสามารถในการรั่วของหลอดเลือด กระบวนการดังกล่าวนำไปสู่การทำลายกำแพงกั้นระหว่างเลือดกับสมอง (blood–brain barrier; BBB) ทำให้ไวรัสสามารถเข้าสู่ระบบประสาทส่วนกลาง และก่อให้เกิดสมองอักเสบรุนแรง (encephalitis) ขณะเดียวกันการติดเชื้อในระบบทางเดินหายใจและหลอดเลือดปอดส่งผลให้เกิดการบาดเจ็บของเนื้อเยื่อปอดและภาวะหายใจล้มเหลวเฉียบพลัน (acute respiratory distress syndrome; ARDS) การดำเนินโรคที่รุนแรงร่วมกับการอักเสบและความผิดปกติของระบบหลอดเลือด เป็นสาเหตุสำคัญที่ทำให้โรคติดเชื้อไวรัสนิปาห์มีอัตราการเสียชีวิตสูงประมาณร้อยละ 40–75
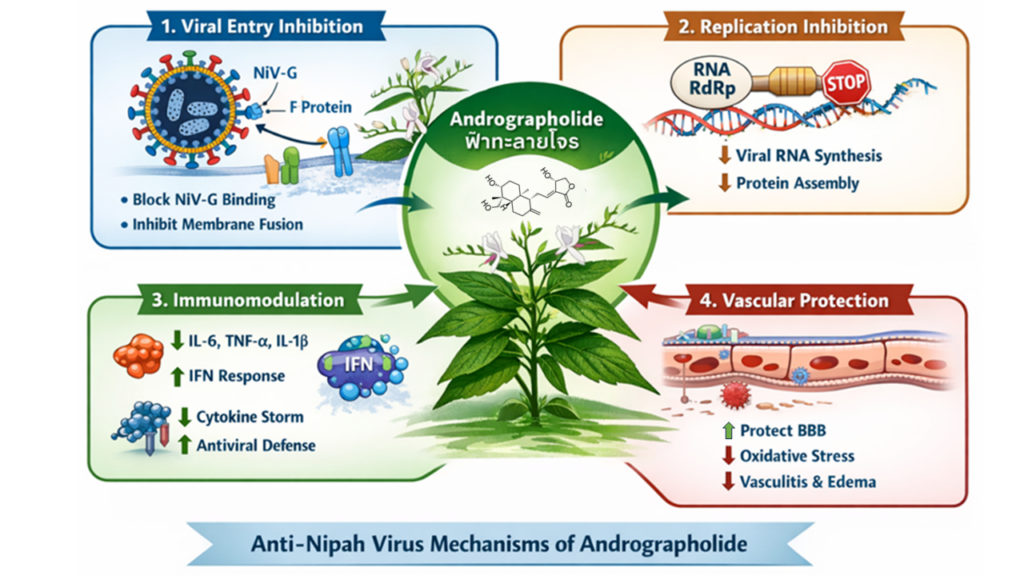
ภาพที่ 2 กลไกที่เป็นไปได้ของสารแอนโดรกราโฟไลด์ (andrographolide) ซึ่งมีอยู่ในสมุนไพรฟ้าทะลายโจรที่สามารถยับยั้งและลดอาการของการติดเชื้อไวรัสนิปาห์โดยผ่านกลไกที่เป็นไปได้ดังนี้ 1. การยับยั้งไวรัสเข้าเซลล์ผ่านการจับโปรตีนบนผิวเซลล์ 2. การรบกวนการทำงานของเอนไซม์ที่ใช้ในการเพิ่มจำนวนไวรัส 3. ลดการหลั่งสารกระตุ้นการอักเสบและกระตุ้นกลไกการป้องกันไวรัสนิปาห์ 4. การป้องกันไวรัสผ่าน blood brain barrier และ ลด oxidative stress ซึ่งช่วยลดอาการสมองอักเสบและหลอดเลือดอักเสบ
ฟ้าทะลายโจร หรือ Andrographis paniculata (Burm. f.) Nees (วงศ์ Acanthaceae) เป็นสมุนไพรสำคัญในแพทย์แผนไทยและเอเชียตะวันออกเฉียงใต้ มีสารออกฤทธิ์หลักคือ แอนโดรกราโฟไลด์ ซึ่งได้รับการศึกษากว้างขวางด้านฤทธิ์ต้านไวรัส ต้านการอักเสบ และกระตุ้นภูมิคุ้มกัน จากการศึกษาทดลองที่ดำเนินการโดยคอมพิวเตอร์ (in silico) พบว่า สารแอนโดรกราโฟไลด์ มีศักยภาพเชิงกลไกในการยับยั้งไวรัสนิปาห์ทั้งทางตรงและทางอ้อม ผ่านการรบกวนการเข้าสู่เซลล์ไวรัส (viral entry) โดยแทรกตัวเข้าบริเวณ receptor-binding domain (RBD-like protein) หรือ glycoprotein interface และลด binding affinity ของโปรตีนไวรัสกับตัวรับ ephrin-B2 และ ephrin-B3 บนผิวเซลล์เจ้าบ้าน ส่งผลให้ลดจำนวนไวรัส (viral load) รวมถึงลดประสิทธิภาพของกระบวนการหลอมรวมของเยื่อหุ้มระหว่างไวรัสกับเซลล์ ทำให้ไวรัสไม่สามารถปล่อยสารพันธุกรรมเข้าสู่ภายในเซลล์ได้อย่างสมบูรณ์ และแอนโดรกราโฟไลด์ อาจยับยั้งการเพิ่มจำนวนของไวรัส โดยรบกวนการทำงานของเอนไซม์ RNA-dependent RNA polymerase (RdRp) ส่งผลให้การสังเคราะห์สารพันธุกรรมของไวรัส และการสร้างโปรตีนโครงสร้างลดลง จึงทำให้การประกอบอนุภาคไวรัสใหม่ไม่มีประสิทธิภาพ
นอกจากนี้ จากการศึกษาฤทธิ์ของสารแอนโดรกราโฟไลด์ ยังพบว่า มีความสามารถในการควบคุมการอักเสบของเซลล์เจ้าบ้าน (host cell) โดยลดการอักเสบผ่านทางโปรตีน NF-κB, MAPK, IL-6, TNF-α และ IL-1β ซึ่งทำให้สามารถลดอาการไข้ ปรับสมดุลการตอบสนองของระบบภูมิคุ้มกันของเซลล์เจ้าบ้าน และยับยั้งการกระตุ้นสัญญาณ NF-κB และ MAPK pathways ซึ่งนำไปสู่การลดการหลั่งสารกระตุ้นการอักเสบ เช่น IL-6, TNF-α และ IL-1β พร้อมทั้งช่วยฟื้นฟูการทำงานของ interferon signaling ที่มีบทบาทสำคัญในการต้านไวรัส ตลอดจนอาจลดความเสี่ยงต่อการเกิดการอักเสบในสมอง ปอด และการอักเสบเชิงระบบ (cytokine storm) ซึ่งศักยภาพของสารแอนโดรกราโฟไลด์ในฟ้าทะลายโจรยังสามารถใช้ได้ในโรคที่เกิดจากการติดเชื้อไวรัสชนิดอื่นๆ ด้วย เช่น ไข้หวัดใหญ่ โควิด-19 รวมถึงไข้หวัดตามฤดูกาล ซึ่งสมุนไพรฟ้าทะลายโจรทำงานในลักษณะของสารต้านไวรัสแบบหลายเป้าหมาย (multi-target antiviral agent) ที่ผสานการยับยั้งไวรัสโดยตรง ร่วมกับการควบคุมการอักเสบ และการปกป้องอวัยวะสำคัญของร่างกาย
สมุนไพรและสารจากพืชสมุนไพรเป็นแหล่งของสารออกฤทธิ์ทางชีวภาพ (phytochemicals) ที่หลากหลาย งานวิจัยจำนวนมากรายงานว่า สารเหล่านี้มีฤทธิ์ต้านไวรัส ต้านการอักเสบ และต้านอนุมูลอิสระ ซึ่งอาจช่วยลดความรุนแรงของการติดเชื้อหรือการอักเสบที่เกิดขึ้นในร่างกายได้ ในช่วงเวลาที่ผ่านมา มีการนำเทคนิคที่ทำในห้องปฏิบัติการทดลอง (in vitro) และการวิเคราะห์ทดลองทางคอมพิวเตอร์ (in silico) มาใช้คัดกรองสารจากสมุนไพรเพื่อประเมินความสามารถในการยับยั้งโปรตีนหรือกระบวนการสำคัญของไวรัส อย่างไรก็ตาม หลักฐานเหล่านี้ยังอยู่ในระยะเริ่มต้นและไม่สามารถสรุปเชิงการรักษาได้
การนำเสนอข้อมูลเกี่ยวกับสมุนไพรจำเป็นต้องอยู่บนพื้นฐานของหลักฐานทางวิทยาศาสตร์และไม่ก่อให้เกิดความเข้าใจผิด ซึ่งประเด็นที่สำคัญคือ การใช้ขนาดยาที่เหมาะสมกับโรคและระยะเวลาของการใช้สมุนไพร เช่น ฟ้าทะลายโจร จำเป็นต้องมีการศึกษาและวิเคราะห์ข้อมูลเพิ่มเติม แต่ในกรณีภาวะฉุกเฉิน อาจจะใช้ขนาดยาของฟ้าทะลายโจร โดยเทียบเคียงกับขนาดที่ใช้ในโรคโควิด-19 ไปพลางก่อนได้
บทความนี้ มีวัตถุประสงค์เพื่อทบทวนองค์ความรู้เกี่ยวกับศักยภาพของสมุนไพรบางชนิด ที่มีรายงานความเป็นไปได้ของฤทธิ์ต้านไวรัส ต้านการอักเสบ หรือเสริมภูมิคุ้มกัน ซึ่งอาจมีความเกี่ยวข้องเชิงทฤษฎีกับการติดเชื้อไวรัสนิปาห์ พร้อมทั้งอภิปรายข้อจำกัดและทิศทางการวิจัยในอนาคต ในเชิงทฤษฎี สารจากสมุนไพรอาจมีบทบาทผ่านกลไกต่างๆ ได้แก่ การรบกวนการเกาะของไวรัสกับเซลล์เจ้าบ้าน การยับยั้งเอนไซม์หรือโปรตีนที่เกี่ยวข้องกับการเพิ่มจำนวนของไวรัส และการลดการอักเสบจากการติดเชื้อ ซึ่งเป็นปัจจัยสำคัญของความรุนแรงของโรค และ กลไกเหล่านี้ยังต้องการการพิสูจน์ในระบบชีวภาพที่ซับซ้อนมากขึ้น อย่างไรก็ตาม การป้องกัน การเฝ้าระวัง และการรักษาตามแนวทางการแพทย์แผนปัจจุบันยังคงเป็นหัวใจสำคัญ ในอนาคต การศึกษาต่อยอดพืชสมุนไพรในการต้านไวรัสในระดับโมเลกุล สัตว์ทดลอง และการทดลองทางคลินิก จะมีบทบาทสำคัญในการประเมินศักยภาพที่แท้จริงของสมุนไพรในบริบทของโรคอุบัติใหม่นี้
เอกสารอ้างอิง
Hidalgo, M. A., Romero, A., Figueroa, J., Cortés, P., Concha, I. I., & Hancke, J. L. (2005). Andrographolide interferes with binding of nuclear factor-κB to DNA in HL-60-derived neutrophilic cells. British Journal of Pharmacology, 144(5), 680–686.
Negrete, O. A., Levroney, E. L., Aguilar, H. C., Bertolotti-Ciarlet, A., Nazarian, R., Tajyar, S., & Lee, B. (2005). EphrinB2 is the entry receptor for Nipah virus, an emergent deadly Paramyxovirus. Nature, 436(7049), 401–405.
Lee, B., & Ataman, Z. A. (2011). Modes of Paramyxovirus fusion: A henipavirus perspective. Trends in Microbiology, 19(8), 389–399.
Rockx, B., Brining, D., Kramer, J., Callison, J., Ebihara, H., Mansfield, K., & Feldmann, H. (2011). Clinical outcome of Henipavirus infection in hamsters is determined by the route and dose of infection. Journal of Virology, 85(15), 7658–7671.
Clayton, B. A., Middleton, D., Bergfeld, J., Haining, J., Arkinstall, R., Wang, L., & Marsh, G. A. (2012). Transmission routes for Nipah virus from Malaysia and Bangladesh. Emerging Infectious Diseases, 18(12), 1983–1993.
Mathieu, C., Guillaume, V., Volchkova, V. A., Pohl, C., Jacquot, F., Looi, R. Y., Wong, K. T., Legras-Lachuer, C., Volchkov, V. E., Lachuer, J., & Horvat, B. (2012). Nonstructural Nipah virus C protein regulates both the early host proinflammatory response and viral virulence. Journal of Virology, 86(19), 10766–10775.
Escaffre, O., Borisevich, V., & Rockx, B. (2013). Pathogenesis of Hendra and Nipah virus infection in humans. Journal of Infectious Diseases, 209(Suppl 2), S122–S130.
Ang, B. S. P., Lim, T. C. C., & Wang, L. (2018). Nipah virus infection. Journal of Clinical Microbiology, 56(6), e01875-17.
Adiguna, S. P., Wijaya, Y. T., Rahmi, E. P., & Kurniawan, F. (2021). Antiviral activities of andrographolide and its derivatives: Mechanism of action and potential application. Viruses, 13(11), 2209.
DeBuysscher, B. L., Scott, D., Thomas, T., Feldmann, H., & Prescott, J. (2021). Nipah virus efficiently replicates in human smooth muscle cells. Cells, 10(6), 1319.
Cai, Q., Lin, Y., Shi, S., & Huang, Y. (2022). Andrographolide: A review of its pharmacology, mechanisms of action, and therapeutic potential. Frontiers in Pharmacology, 13, 920435.
Devnath, P., Uddin, M. H., Hossain, M. E., & Chakraborty, A. (2022). Pathogenesis of Nipah virus infection: A review. Microbial Pathogenesis, 170, 105687.
Mandal, M., & Mandal, S. (2024). Discovery of multitarget-directed small molecule inhibitors from Andrographis paniculata for Nipah virus disease therapy: Molecular docking, molecular dynamics simulation and ADME-Tox profiling. Chemical Physics Impact, 8, 100493.
Malarvizhi, G. L., & Bayry, J. (2025). Rationally designed functionalized phytochemical-conjugated fullerene quantum dots inhibiting viral chaperone activity and RNA-dependent RNA polymerase in Nipah virus. FASEB Journal, 39(15), e70890.
Ren, Z., Chen, Z., Xie, Y., & Coghi, P. (2025). Andrographolide and its derivatives: A comprehensive review of anti-infective properties and clinical potential. Molecules, 30(21), 4273.
 Center of Excellence on Environmental Health and Toxicology (EHT)
Center of Excellence on Environmental Health and Toxicology (EHT)










