แคดเมียม (Cadmium; Cd) เป็นโลหะหนักชนิดหนึ่งที่ไม่มีกลิ่น มีจุดหลอมละลาย (melting point) เท่ากับ 321°C และจุดเดือด (boiling point) เท่ากับ 765°C (Faroon et al. 2012) แคดเมียมเป็นโลหะที่ไม่ละลายน้ำ แต่จะละลายได้ดีในสภาวะที่เป็นกรดหรือเมื่ออยู่ในรูปของสารประกอบของเกลือ เช่น แคดเมียมซัลเฟต แคดเมียมคลอไรด์ เป็นต้น นอกจากนี้แคดเมียมสามารถอยู่ในรูปของฝุ่นหรือไอระเหยที่เกิดจากอุตสาหกรรมที่มีการอบ เผา เชื่อม หลอม ผสมหรือเคลือบด้วยแคดเมียมการนำแคดเมียมมาใช้ประโยชน์ ได้แก่ การชุบโลหะ การผสมกับโลหะอื่นเป็นโลหะผสม การผลิตแบตเตอรี่ การใช้เป็นเม็ดสี การใช้ผสมเป็นสารฆ่าเชื้อรา เป็นต้น แคดเมียมมีอยู่ตามธรรมชาติและในอุตสาหกรรมเหมืองแร่ จะเป็นกากแร่ซึ่งเกิดจากการถลุงตะกั่ว ทองแดง หรือสังกะสี จึงทำให้แคดเมียมสามารถปนเปื้อนเข้าสู่สิ่งแวดล้อมได้ นอกจากนี้แคดเมียมยังปนเปื้อนมากับการผลิตปุ๋ยฟอสเฟตจากหินฟอสฟอไรต์ (Phosphorite) และอะพาไทต์ (Apatite) ได้อีกด้วย การปนเปื้อนแคดเมียมในสิ่งแวดล้อมทำให้พืชสามารถดูดซึมแคดเมียมจากดิน น้ำ หรือปุ๋ย และเข้าสู่ห่วงโซ่อาหาร จนถึงสัตว์และมนุษย์ได้ในลำดับต่อไป
แคดเมียมสามารถเข้าสู่ร่างกายได้ โดยการหายใจเอาฝุ่นหรือควันของแคดเมียมเข้าสู่ร่างกาย เช่น การทำงานในอุตสาหกรรมดังกล่าวข้างต้น การสัมผัสควันบุหรี่ หรือการบริโภคน้ำหรืออาหารที่ปนเปื้อนแคดเมียม องค์การอนามัยโลก (WHO) ได้กำหนดปริมาณแคดเมียมสูงสุดในน้ำดื่มไม่เกิน 0.003 มิลลิกรัมต่อลิตรหรือส่วนในล้านส่วน (ppm; part per million) ในขณะที่สำนักงานปกป้องสิ่งแวดล้อมแห่งสหรัฐอเมริกา (USEPA) ได้กำหนดระดับแคดเมียมปนเปื้อนสูงสุดในน้ำดื่มไว้ที่ 0.005 มิลลิกรัมต่อลิตร นอกจากนี้ WHO ได้กำหนดปริมาณแคดเมียมสูงสุดในอาหารชนิดต่างๆไว้ ตัวอย่างเช่น ในผักไม่เกิน 0.2 มิลลิกรัมต่อกิโลกรัม ในข้าวไม่เกิน 0.4 มิลลิกรัมต่อกิโลกรัม ในเนื้อสัตว์ไม่เกิน 0.05 มิลลิกรัมต่อกิโลกรัม ในตับหมู/วัว ไม่เกิน 1.25 มิลลิกรัมต่อกิโลกรัม ในปลาไม่เกิน 1 มิลลิกรัมต่อกิโลกรัม และในสัตว์ทะเลชนิดมีเปลือก (Molluscs) ไม่เกิน 2.0 มิลลิกรัมต่อกิโลกรัม โดยเมื่อได้รับแคดเมียมเข้าสู่ร่างกายจะสามารถสะสมในเลือดได้เป็นเวลา 3 – 4 เดือน แต่สามารถสะสมอยู่ในอวัยวะต่างๆในร่างกาย (biological half-life) ได้นานถึง 30 ปี
จากงานวิจัยของห้องปฏิบัติการวิจัยเภสัชวิทยา สถาบันวิจัยจุฬาภรณ์ และศูนย์ความเป็นเลิศด้านอนามัยสิ่งแวดล้อมและพิษวิทยา ซึ่งได้ทำการศึกษาหาปริมาณแคดเมียมในตัวอย่างน้ำและอาหารชนิดต่างๆระหว่างปี พ.ศ. 2548 – 2551 (Nookabkaew et al., 2013) และมีการศึกษาเพิ่มเติมอีกในช่วงปี พ.ศ. 2552 – 2566 ซึ่งเป็นข้อมูลภายในหน่วยงานฯ (unpublished data) เพื่อติดตามสถานการณ์การปนเปื้อนของโลหะที่เป็นพิษ (Toxic metals) โดยเก็บตัวอย่างน้ำจำนวน 504 ตัวอย่าง ได้แก่ น้ำแม่น้ำ น้ำประปา น้ำดื่มบรรจุขวด น้ำสำหรับการเพาะปลูก รวมถึงน้ำทะเล พบว่า มีปริมาณแคดเมียมน้อยกว่า 0.05 ไมโครกรัมต่อลิตรหรือส่วนในพันล้านส่วน (ppb; part per billion) ยกเว้นตัวอย่างน้ำบริเวณใกล้เคียงกับโรงงานอุตสาหกรรมบางพื้นที่ ที่ตรวจพบปริมาณแคดเมียมในช่วง 1 – 2.5 ไมโครกรัมต่อลิตร ซึ่งตัวอย่างน้ำทั้งหมดยังคงมีปริมาณแคดเมียมต่ำกว่าที่ WHO กำหนด
ส่วนในตัวอย่างดินจากพื้นที่เกษตรกรรมจำนวน 203 ตัวอย่าง พบแคดเมียม 0.012 – 0.753 มิลลิกรัมต่อกิโลกรัม โดยมีปริมาณเฉลี่ยที่ 0.142 มิลลิกรัมต่อกิโลกรัม ซึ่งปริมาณแคดเมียมในดินในประเทศไทยมีค่าพื้นฐานที่ 0.15 มิลลิกรัมต่อกิโลกรัม (Zarcinas et. al, 2004)
ทางคณะผู้วิจัยได้ทำการเก็บตัวอย่างอาหารสัตว์ชนิดต่างๆ เช่น อาหารปลา ไก่ เป็ด กุ้ง จำนวนทั้งสิ้น 155 ตัวอย่าง พบว่า มีปริมาณแคดเมียมในช่วง 0.003 – 1.635 มิลลิกรัมต่อกิโลกรัม โดยอาหารสัตว์ที่มีแคดเมียมสูงที่สุดคือ อาหารกุ้ง (เฉลี่ย 0.505 มิลลิกรัมต่อกิโลกรัม)
นอกจากนี้ยังได้ทำการเก็บตัวอย่างอาหารจากตลาดสดทั่วไป ได้แก่ ตัวอย่างผัก จำนวน 327 ตัวอย่าง มีปริมาณแคดเมียมในช่วง น้อยกว่า 0.004 – 0.372 มิลลิกรัมต่อกิโลกรัม โดยมีปริมาณเฉลี่ย 0.014 มิลลิกรัมต่อกิโลกรัม ในจำนวนนี้มีผัก 2 ตัวอย่างที่ตรวจพบปริมาณแคดเมียมเกินมาตรฐาน (มากกว่า 0.2 มิลลิกรัมต่อกิโลกรัม) ตัวอย่างอาหารทะเลจำนวน 410 ตัวอย่าง มีปริมาณแคดเมียมในช่วง น้อยกว่า 0.002 – 15.79 มิลลิกรัมต่อกิโลกรัม โดยพบปริมาณเฉลี่ยสูงที่สุดในหอยเชลล์ (3.31 มิลลิกรัมต่อกิโลกรัม) รองลงมาคือ หอยหมาก (1.55 มิลลิกรัมต่อกิโลกรัม) ส่วนตัวอย่างกุ้งและปลาตรวจพบแคดเมียมน้อยกว่า 0.2 มิลลิกรัมต่อกิโลกรัม จากข้อมูลปริมาณแคดเมียมในอาหารทะเลพบว่า มีจำนวน 15 ตัวอย่าง จาก 410 ตัวอย่าง คิดเป็นร้อยละ 3.6 (3.6%) ที่มีปริมาณแคดเมียมเกินค่ามาตรฐาน (มากกว่า 2 มิลลิกรัมต่อกิโลกรัม) สำหรับตัวอย่างข้าวขาว/ข้าวกล้องและข้าวสีรวม 426 ตัวอย่าง มีปริมาณแคดเมียมเฉลี่ย 0.020 มิลลิกรัมต่อกิโลกรัม โดยไม่มีตัวอย่างข้าวที่พบแคดเมียมเกินค่ามาตรฐาน (ตารางที่ 1)
ตารางที่ 1 ปริมาณของแคดเมียมในสิ่งแวดล้อมและอาหาร ระหว่างปี พ.ศ.2548-2566 (จำนวน 2,025 ตัวอย่าง)
| ชนิดของตัวอย่าง | จำนวนตัวอย่าง | ปริมาณแคดเมียมที่พบ | หมายเหตุ |
| น้ำ (น้ำแม่น้ำ น้ำประปา น้ำดื่มบรรจุขวด น้ำเพาะปลูก น้ำทะเล) | 504 | น้อยกว่า 0.05 ไมโครกรัมต่อลิตร (ยกเว้น ตัวอย่างน้ำบริเวณใกล้เคียงโรงงานบางแห่ง 1.0-2.5 ไมโครกรัมต่อลิตร) | ตัวอย่างน้ำทั้งหมดมีปริมาณแคดเมียมต่ำกว่ามาตรฐาน WHO (น้อยกว่า 3 ไมโครกรัมต่อลิตร หรือ 0.003 มิลลิกรัมต่อลิตร) |
| ดิน (พื้นที่เกษตรกรรม) | 203 | 0.012-0.753 มิลลิกรัมต่อกิโลกรัม (เฉลี่ย 0.142 มิลลิกรัมต่อกิโลกรัม) | ปริมาณแคดเมียมในดินในประเทศไทย มีค่าพื้นฐานเท่ากับ 0.15 มิลลิกรัมต่อกิโลกรัม |
| อาหารสัตว์ (ปลา ไก่ เป็ด กุ้ง) | 155 | 0.003-1.635 มิลลิกรัมต่อกิโลกรัม | แคดเมียมสูงที่สุดในอาหารกุ้ง เฉลี่ย 0.505 มิลลิกรัมต่อกิโลกรัม (สหภาพยุโรปกำหนดมาตรฐานแคดเมียมในอาหารปลาไม่เกิน 1 มิลลิกรัมต่อกิโลกรัม, 2002/32/EC) |
| ผักสดในตลาด | 327 | น้อยกว่า 0.004-0.372 มิลลิกรัมต่อกิโลกรัม(เฉลี่ย 0.14 มิลลิกรัมต่อกิโลกรัม) | มี 2 ตัวอย่าง ที่มีแคดเมียมเกินค่ามาตรฐาน (มากกว่า 0.2 มิลลิกรัมต่อกิโลกรัม) |
| อาหารทะเล | 410 | น้อยกว่า 0.002-15.79 มิลลิกรัมต่อกิโลกรัม | มี 15 ตัวอย่าง ที่มีแคดเมียมเกินค่ามาตรฐาน (มากกว่า 2.0 มิลลิกรัมต่อกิโลกรัม) |
| ข้าวกล้อง ข้าวสี ข้าวขาว | 426 | เฉลี่ย 0.020 มิลลิกรัมต่อกิโลกรัม | ไม่มีตัวอย่างใดที่มีแคดเมียมเกินค่ามาตรฐาน WHO (น้อยกว่า 0.4 มิลลิกรัมต่อกิโลกรัม) |
นอกจากนี้ ห้องปฏิบัติการวิจัยเภสัชวิทยายังได้ทำการศึกษาความเป็นพิษของแคดเมียม โดยศึกษาความเป็นพิษต่อหลอดเลือดในหนูแรท ที่ได้รับแคดเมียมในน้ำดื่มที่มีความเข้มข้น 1, 10 และ 50 มิลลิกรัมต่อลิตร แบบกึ่งเรื้อรังเป็นเวลานาน 3 เดือน ผลที่ได้พบว่า ค่าความดันโลหิตซิสโตลิก (Systolic blood pressure) ในกลุ่มที่ได้รับแคดเมียมในน้ำดื่มที่ปริมาณ 10 และ 50 มิลลิกรัมต่อลิตร เพิ่มขึ้นอย่างมีนัยสำคัญประมาณ 20–30% ของกลุ่มควบคุมที่ได้รับน้ำดื่มสำหรับสัตว์ทดลอง (Yoopan et al, 2006, 2008)
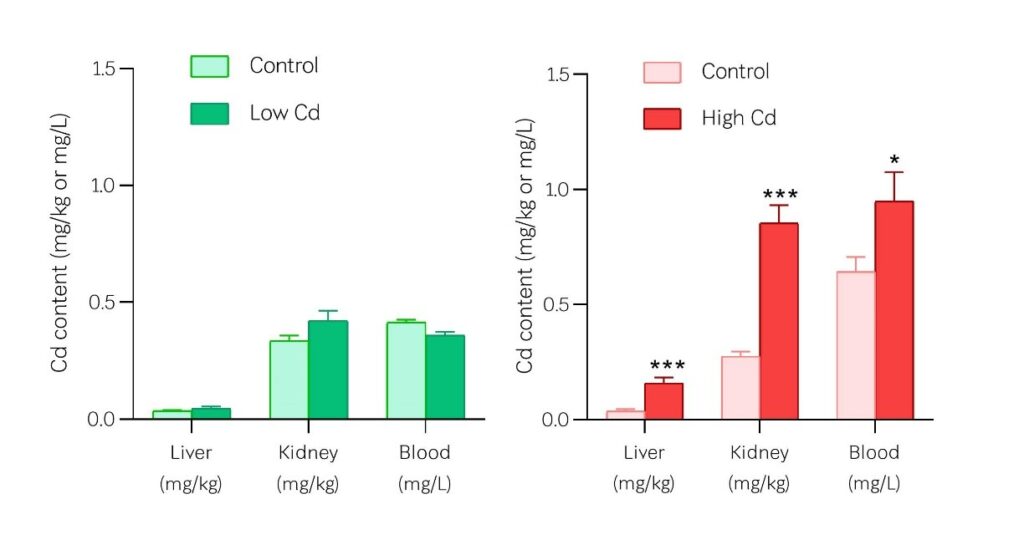
คณะผู้วิจัยยังได้มีงานวิจัย ในการศึกษาผลของการได้รับสัมผัสแคดเมียมต่อระบบภูมิต้านทานของร่างกายในสัตว์ทดลองแบบเรื้อรัง โดยให้หนูแรทได้รับน้ำดื่มที่มีปริมาณความเข้มข้นของสารละลายแคดเมียมคลอไรด์ 0.05 มิลลิกรัมต่อลิตร (เทียบเท่าปริมาณในคน 0.008 มิลลิกรัมต่อลิตร ซึ่งสูงกว่าค่ามาตรฐานที่ WHO กำหนดปริมาณแคดเมียมสูงสุดในน้ำดื่มไว้ที่ 0.003 มิลลิกรัมต่อลิตร) และ 0.006 มิลลิกรัมต่อลิตร (เทียบเท่าปริมาณในคน 0.001 มิลลิกรัมต่อลิตร) เป็นเวลา 4 และ 6 เดือน ตามลำดับ ผลการทดลองพบว่า ในกลุ่มหนูแรทที่ได้รับแคดเมียมในน้ำดื่มที่ปริมาณ 0.05 มิลลิกรัมต่อลิตร ระยะเวลานาน 4 เดือน มีการลดลงของการทำงานของระบบภูมิคุ้มกันชนิดทีเซลล์ (T-cells) ซึ่งมีบทบาทและหน้าที่ในการกำจัดเซลล์ที่ติดเชื้อโรคและช่วยกระตุ้นภูมิต้านทานอื่นๆในร่างกายให้ดีขึ้น ในขณะที่หนูแรทที่ได้รับแคดเมียมในน้ำดื่มที่ปริมาณ 0.006 มิลลิกรัมต่อลิตร ระยะเวลานาน 6 เดือน ไม่พบการเปลี่ยนแปลงต่อระบบภูมิคุ้มกันอย่างมีนัยสำคัญทางสถิติ (Suntararuks et al., 2008) ซึ่งผลการทดลองดังกล่าวนี้สอดคล้องกับปริมาณแคดเมียมที่ปนเปื้อนในน้ำดื่มที่หนูแรทได้รับ นอกจากนี้ยังพบปริมาณแคดเมียมที่สะสมในอวัยวะของหนูแรทเพิ่มขึ้น คือ ตับ ไต และเลือด ซึ่งกลุ่มหนูแรทที่ได้รับแคดเมียมในน้ำดื่มที่ปริมาณสูง 0.05 มิลลิกรัมต่อลิตร (High Cd) จะมีปริมาณแคดเมียมสะสมในตับ ไต และเลือด สูงกว่ากลุ่มควบคุมอย่างมีนัยสำคัญทางสถิติ (รูปที่ 1) ส่วนกลุ่มหนูแรทที่ได้รับแคดเมียมในปริมาณต่ำ 0.006 มิลลิกรัมต่อลิตร (Low Cd) พบการสะสมของแคดเมียมในร่างกายไม่แตกต่างจากกลุ่มควบคุม (แคดเมียมที่พบสะสมนี้อาจมาจากอาหารหนูที่กินเข้าสู่ร่างกาย) จากผลการทดลองดังกล่าวนี้ จะเห็นได้ว่าความเป็นพิษของแคดเมียม เกิดจากปริมาณแคดเมียมที่ได้รับเข้าสู่ร่างกายและระยะเวลาการสัมผัส เมื่อได้รับแคดเมียมเข้าสู่ร่างกายในรูปแบบน้ำดื่ม หรืออาหารที่ปนเปื้อนแคดเมียมในปริมาณสูง (ปริมาณแคดเมียมเกินค่ามาตรฐานที่ WHO กำหนดไว้) เป็นระยะเวลานานๆ อาจทำให้เกิดการสะสมในร่างกายและเกิดความเป็นพิษได้โดยเฉพาะทำให้มีการสะสมแคดเมียมสูงที่ไต ซึ่งอาจจะทำให้เกิดการอักเสบของไตและเกิดภาวะไตวายเรื้อรังได้ นอกจากนี้ แคดเมียมยังไปสะสมที่กระดูก ซึ่งอาจทำให้เกิดโรคกระดูกพรุน กระดูกบาง มีอาการปวดกระดูกอย่างมากโดยเฉพาะที่กระดูกสะโพก ซึ่งเป็นอาการของโรคที่เกิดจากพิษของแคดเมียมที่เรียกว่า ‘โรคอิไต-อิไต’ (https://www.hfocus.org/content/2024/04/30203. สืบค้นเมื่อวันที่ 12 เม.ย. 2567)
รูปที่ 1 ปริมาณแคดเมียมที่สะสมในตับ (Liver) ไต (Kidney) และเลือด (Blood) ของสัตว์ทดลองที่ได้รับแคดเมียม (Cd) ในรูปแบบน้ำดื่มที่ปริมาณ 0.05 มิลลิกรัมต่อลิตร (High) ระยะเวลา 4 เดือน และแคดเมียมในน้ำดื่มที่ปริมาณ 0.006 มิลลิกรัมต่อลิตร (Low) ระยะเวลา 6 เดือน เทียบกับกลุ่มควบคุมที่ได้รับน้ำดื่มสำหรับสัตว์ทดลอง (Reverse osmosis)
* มีความแตกต่างอย่างมีนัยสำคัญทางสถิติเมื่อเทียบกับกลุ่มควบคุม (Control)
เอกสารอ้างอิง
- Cadmium – Environmental Protection Agency. https://www.epa.gov/ground-water-and-drinking-water/national-primary-drinking-water-regulations.
- Directive 2002/32/EC of the European parliament and of the council of 7 May 2002 on undesirable substances in animal feed.
- Faroon, O., Ashizawa, A., Wright, S., Tucker, P., Jenkins, K. Ingerman, L. and Rudisill, C. 2012. Toxicological profile for cadmium. Atlanta (GA): Agency for Toxic Substances and Disease Registry (US).
- Nookabkaew, S., Rangkadilok, N., Akib, C.A., Tuntiwigit, N., Saehun, J. and Satayavivad J. 2013. Evaluation of trace elements in selected foods and dietary intake by young children in Thailand. Food Additives & Contaminants: Part B, 6, 55 – 67.
- Suntararuks, S., Yoopan, N., Rangkadilok, N., Worasuttayangkurn, L., Nookabkaew, S., and Satayavivad, J. 2008. Immunomodulatory effects of cadmium and Gynostemma pentaphyllum herbal tea on rat splenocyte proliferation. Journal of Agricultural and Food Chemistry, 56(19), 9305–9311.
- Yoopan, N., Wongsawatkul, O., Watcharasit, P., Piyachaturawat. P., and Satayavivad, J. 2006. Contribution of cholinergic muscarinic functions in cadmium-induced hypertension in rats Toxicology Letters, 164, S155.
- Yoopan, N., Watcharasit, P., Wongsawatkul, O., Piyachaturawat, P., and Satayavivad, J. 2008. Attenuation of eNOS expression in cadmium-induced hypertensive rats. Toxicology Letters, 176(2), 157–161.
- Zarcinas, B.A., Pongsakul P., McLaughlin, M.J., and Cozens, G. 2004. Heavy metals in soils and crops in Southeast Asia. 2. Thailand. Environmental Geochemistry and Health, 26, 359–371.
 Center of Excellence on Environmental Health and Toxicology (EHT)
Center of Excellence on Environmental Health and Toxicology (EHT)